Ewa Orlewska1, 2
Analiza efektywności kosztów przedłużonej profilaktyki przeciwzakrzepowej enoksaparyną u chorych poddanych zabiegowi planowanej alloplastyki stawu biodrowego w Polsce
The cost-effectiveness analysis of extended venous thromboembolism prophylaxis with enoxaparin versus short-term prophylaxis after elective hip replacement in Poland.
1 Centrum Farmakoekonomiki, Warszawa
2 Katedra i Zakład Farmakologii Doświadczalnej i Klinicznej AM w Warszawie
Streszczenie
Cel: Celem pracy jest ocena kosztów i efektów przedłużonej poszpitalnej profilaktyki enoksaparyną w porównaniu do profilaktyki stosowanej tylko w okresie hospitalizacji u chorych poddanych zabiegowi planowanej alloplastyki stawu biodrowego w Polsce.
Metody: Analizę efektywności kosztów przeprowadzono techniką modelowania. W modelu wykorzystano publikowane dane z międzynarodowych badań klinicznych i epidemiologicznych oraz odpowiadające polskim warunkom dane o zużytych zasobach i cenach jednostkowych. Wiek badanej populacji wynosił 70 lat, 58% stanowiły kobiety. Analizę przeprowadzono z perspektywy płatnika, uwzględniając tylko bezpośrednie koszty medyczne. Miarą efektywności były zyskane lata życia, skalkulowane na podstawie dostępnych dowodów na temat wpływu enoksaparyny na zmniejszenie ryzyka choroby zakrzepowo-zatorowej po alloplastyce stawu biodrowego. W celu określenia opłacalności koszt uzyskania dodatkowego roku życia porównano z hipotetyczną granicą opłacalności leczenia w Polsce, obliczoną na podstawie rocznego kosztu dializoterapii (60 000 zł). Przeprowadzono jednokierunkowe analizy wrażliwości oraz analizy scenariuszy.Wyniki: W hipotetycznej kohorcie 100 chorych po zabiegu alloplastyki stawu biodrowego oczekiwany koszt i wynik wynoszą 53470 zł i 1269.4 lata dla przedłużonej i 33190 zł i 1248.2 lat dla standardowej profilaktyki enoksaparyną. Koszt uzyskania dodatkowego roku życia dzięki zastosowaniu przedłużonej profilaktyki enoksaparyną wynosi więc 954 zł (1811 zł po zdyskontowaniu przy użyciu 5% stopy dyskontowania) i w żadnym przypadku analizowanym w jednokierunkowych analizach wrażliwości oraz analizach scenariuszy nie przekraca wartości 3000 zł/dodatkowy rok życia.Wniosek: U chorych poddanych zabiegowi planowanej alloplastyki stawu biodrowego przedłużona poszpitalna profilaktyka enoksaparyną jest strategią bardziej skuteczną oraz wysoce opłacalną w porównaniu do profilaktyki stosowanej tylko w okresie hospitalizacji.
Summary
Evidence-based medicine guidelines based on venographic end points recommend extended venous thromboembolism (VTE) prophylaxis with low-molecular-weight heparin (LMWH) in patients having elective hip surgery. The aim of the study was to estimate the expected cost-effectiveness of such prophylaxis with enoxaparin administered for 21 days postdischarge vs. using enoxaparin for hospital admission only.Methods: Decision analysis model was developed to combine probability data estimated from published literature and Polish data on resource use and unit cost. Target population was people aged 70, 58% women. The perspective of health-care payer´s was adopted and only direct medical costs were analysed. The outcome measures were life years gained (LYG), calculated on the basis of available evidence for a preventive effect of enoxaparin on VTE risk after elective hip replacement. Incremental cost-effectiveness ratio was calculated to provide estimates of the cost per life year gained. The cost-effectiveness threshold was calculated on the basis of 1-year haemodialysis treatment cost (60000 PLN, 1 EUR=4 PLN; in 2003). The one-way and scenario sensitivity analyses were performed.
Results: For hypothetical cohort of 100 patient undergoing elective hip replacement the expected cost and outcome were 53470 PLN and 1269.4 LY for extended and 33190 PLN and 1248.2 LY for standard enoxaparin as prophylaxis for VTE. For the extended enoxaparin group this translated to 952 PLN/LYG. A series of one-way and scenario analyses showed modest change in cost/LYG. In no instance did the ICER exceed 3000 PLN/LYG.Conclusion: Prolonged enoxaparin prophylaxis after elective hip replacement is more effective than conventional short term prophylaxis in terms of LYG and also appears to be clearly cost-effective, using Polish cost data.

Wstęp
Żylna choroba zakrzepowo-zatorowa (venous thromboembolism, VTE) obejmuje zakrzepicę żył głębokich (deep venous thrombosis, DVT) oraz zator tętnicy płucnej (pulmonary embolism, PE). Przyczyną DVT jest powstanie zakrzepu w żyłach kończyn dolnych, przyczyną PE jest zazwyczaj ulokowanie się fragmentu tego zakrzepu w tętnicy płucnej. Profilaktyka przeciwzakrzepowa skutecznie zmniejsza częstość występowania VTE [1]. Racjonalnymi przesłankami do stosowania profilaktyki VTE są: klinicznie niemy przebieg choroby u większości pacjentów, oraz chorobowość, koszty i potencjalna śmiertelność związana VTE. Objawy zarówno DVT, jak i PE są najczęściej niespecyficzne, dlatego rozpoznanie tych jednostek chorobowych jest bardzo trudne [2,3]. Ponieważ pierwszą manifestacją choroby może być śmiertelny PE, oczekiwanie na objawy a następnie poleganie na diagnostyce i leczeniu VTE nie jest prawidłowym postępowaniem. Nierozpoznana i nieleczona DVT może również powodować w przyszłości zespół pozakrzepowy i predysponować pacjentów do nawrotów VTE [4,5].
Decyzję o zastosowaniu i intensywności profilaktyki przeciwzakrzepowej w różnych specjalnościach medycznych ułatwia znajomość czynników ryzyka i podział chorych na grupy w zależności od stopnia zagrożenia VTE. Do grupy bardzo dużego ryzyka zakrzepowego należą m.in. chorzy poddawani zabiegom ortopedycznym na stawie biodrowym lub kolanowym [6-13]. W oparciu o wyniki badań flebograficznych z zastosowaniem środków cieniujących, przeprowadzonych w grupach kontrolnych lub u chorych randomizowanych do grup otrzymujących placebo stwierdzono, że w ciągu 7-14 dni po zabiegu alloplastyki stawu biodrowego ryzyko wystąpienia DVT wynosi 50-58%, ryzyko wystąpienia proksymalnej DVT – 23-31% [14-25], a u 7-11% badanie scyntygraficzne płuc wskazuje na duże prawdopodobieństwo PE [26,27]. Bez stosowania przedłużonej profilaktyki w ciągu 4-5 tygodni po opuszczeniu szpitala u 10-20% chorych rozpoznano flebograficznie nowe przypadki DVT [27-29], a u około 6% chorych wyniki badanie scyntygraficzne płuc wskazuje na duże prawdopodobieństwo PE [27].
Częstość występowania objawowej i obiektywnie potwierdzonej VTE jest dużo mniejsza niż w przypadku rutynowego wykonywania badań flebograficznych. Na przykład w grupie 1162 chorych, u których wykonano operację alloplastyki stawu biodrowego i u których stosowano tylko pończochy uciskowe, 6-miesięczna skumulowana zapadalność na VTE wynosiła 3,4%: PE stwierdzono u 1,6% (śmiertelny u 0,3%) a DVT u 1,9% [30]. Jednak mimo że większość DVT rozpoznanych flebograficznie przebiega bezobjawowo i ustępuje bez leczenia, zakrzepica rozpoznana w ten sposób pozostaje wciąż wiarygodną miarą wyniku przy porównywaniu skuteczności różnych metod profilaktyki przeciwzakrzepowej.
Zalecenia dotyczące profilaktyki VTE są od wielu lat modyfikowane, głównie w oparciu o wyniki randomizowanych, kontrolowanych badań klinicznych. Według najnowszych zaleceń American College of Chest Physicians [31] w przypadku planowej alloplastyki stawu biodrowego należy stosować heparynę drobnocząsteczkową lub doustny antykoagulant (stopień 1A), alternatywnie heparynę niefrakcjonowaną w dawkach korygowanych (stopień 2A). Jednoczesne stosowanie pończoch elastycznych lub IPC może zwiększyć skuteczność tego postępowania (stopień 2C). Nie zaleca się natomiast stosowania wyłącznie małych dawek niefrakcjonowanej heparyny, kwasu acetylosalicylowego, dekstranu lub IPC. Profilaktyka przeciwzakrzepowa powinna trwać co najmniej 7-10 dni po zabiegu (stopień 1A). Zapobiegawcze stosowanie heparyny drobnocząsteczkowej przez dłuższy czas jest zalecane przynajmniej u chorych z wysokim ryzykiem DVT (stopień 2A).
Polskie wytyczne profilaktyki i leczenia VTE [32, 33] w planowanej alloplastyce stawu biodrowego zalecają stosowanie heparyn drobnocząsteczkowych w dawkach profilaktycznych (stopień 1A). Skuteczność tej profilaktyki może zwiększyć dodatkowe zastosowanie pończoch elastycznych i/lub PUP (stopień 2C). Nie zaleca się stosowania jako profilaktyki: tylko kwasu acetylosalicylowego, heparyny niefrakcjonowanej w dawkach profilaktycznych, dekstranu ani samych metod mechanicznych. Profilaktykę przeciwzakrzepową należy stosować przez co najmniej 7-10 dni (stopień 1A). Przedłużone do 30 dni profilaktyczne stosowanie heparyn drobnocząsteczkowych zaleca się przynajmniej u chorych ze zwiększonym ryzykiem zakrzepowym (stopień 2A). Wytyczne zaakceptowane przez Polskie Środowisko Ortopedyczne zalecają stosowanie heparyn drobnocząsteczkowych w czasie 4 tygodni od zabiegu planowanej alloplastyki stawu biodrowego.
Mimo przekonujących dowodów na konieczność stosowania profilaktyki przeciwzakrzepowej u chorych poddanych zabiegowi alloplastyki stawu biodrowego i sformułowanych w wytycznych schematów postępowania, według oceny Grupy Roboczej d/s Profilaktyki Przeciwzakrzepowej w Polsce tylko 60% ortopedów stosuje profilaktykę zgodnie z obowiązującymi zasadami. Głównym problemem jest czas stosowania profilaktyki – w praktyce zazwyczaj zbyt krótki. Przedłużona profilaktyka heparynami drobnocząsteczkowymi zwiększa koszty związane z zabiegiem planowanej alloplastyki stawu biodrowego, jednocześnie jednak zmniejsza częstość występowania VTE. Analizy farmakoekonomiczne przeprowadzone w Szwecji [34], Francji [35] i Wielkiej Brytanii [36] wykazały, że stosowanie enoksaparyny przez 21 dni po wypisaniu ze szpitala jest opłacalne.
Wyniki badań klinicznych
Skuteczność przedłużonej profilaktyki przeciwzakrzepowej z użyciem heparyn drobnocząsteczkowych u chorych po operacji alloplastyki stawu biodrowego badano w 6 randomizowanych, przeprowadzonych metodą podwójnie ślepej próby badaniach klinicznych, w których miarą wyniku była rozpoznana flebograficznie DVT. Liczba chorych biorących udział w poszczególnych badaniach waha się od 179 do 569. Oceniano skuteczność dwóch LMWH: enoksaparyny [37, 40, 41] i dalteparyny [42-44]. Grupa kontrolna w pięciu badaniach otrzymywała w czasie pobytu w szpitalu profilaktykę z użyciem heparyny drobnocząsteczkowej, a następnie placebo [37, 40-43], w jednym natomiast badaniu w grupie kontrolnej stosowano w czasie pobytu w szpitalu profilaktykę z użyciem warfaryny, a następnie placebo [44]. Profilaktykę z użyciem LMWH w 4 badaniach rozpoczynano przed operacją [37, 40, 42, 43], w jednym badaniu po operacji [41] i w jednym badaniu przed i po operacji [44]. Dawkowanie LMWH odpowiadało dawkom zarejestrowanym w tym wskazaniu, tylko w jednym badaniu dawka początkowa wynosiła połowę zwykle stosowanej dawki [44]. W pięciu badaniach LMWH stosowane były jeden raz dziennie [37, 40, 42-44], w jednym badaniu w okresie pobytu chorego w szpitalu stosowano dawkowanie 2 razy dziennie [41]. Czas pobytu chorych w szpitalu wynosił 6-14 dni, profilaktyka po wypisie chorego ze szpitala trwała 18-29 dni a ocenę jej skuteczności przeprowadzano 27-35 dni po operacji. W 3 badaniach ocenę flebograficzną przeprowadzono dwukrotnie: w dniu wypisu ze szpitala oraz na końcu obserwacji (35 dni po operacji) [40, 42, 44]. W dwóch z tych badań randomizację przeprowadzono w dniu wypisu ze szpitala i na podstawie wyników badania flebgraficznego wykluczono chorych ze stwierdzoną flebograficznie DVT [40] lub wykluczono chorych ze stwierdzoną flebograficznie proksymalną DVT [42].
Zarówno indywidualna analiza wyników wszystkich 6 badań, jak i ich metaanaliza [45], wykazują znamienną redukcję ryzyka DVT po zastosowaniu LMWH w profilaktyce długoterminowej. Według metaanalizy wszystkich 6 badań częstość epizodów rozpoznanej flebograficznie DVT w okresie po opuszczeniu szpitala wynosi w grupie placebo 150/666 chorych (22,5%) a w grupie LMWH 72/911 chorych (7,9%). W celu uniknięcia jednego epizodu DVT należy więc stosować przedłużoną profilaktykę za pomocą LMWH u 8,2 chorych (95% CI: 5,7-14,6; p<0,001) [45]. Statystycznie znamienną redukcję ryzyka proksymalnej DVT wykazano w 3 z 6 badań [37, 41, 44]. Według metaanalizy wszystkich 6 badań częstość epizodów rozpoznanej flebograficznie proksymalnej DVT w okresie po opuszczeniu szpitala wynosi w grupie placebo 76/678 chorych (11,2%) a w grupie LMWH 26/866 chorych (3%). W celu uniknięcia jednego epizodu proksymalnej DVT należy więc stosować przedłużoną profilaktykę za pomocą LMWH u 14,9 chorych (95% CI: 9,3-38,5; p<0,001) [45]. Statystycznie znamienną redukcję ryzyka objawowej DVT po zastosowaniu przedłużonej profilaktyki za pomocą LMWH (1,5% vs 7,6%, RR 0,2; p=0,035) stwierdzono w jednym badaniu [37]. Według metaanalizy wszystkich 6 badań częstość objawowej VTE wynosi w grupie placebo 36/862 (4,2%), a w grupie LMWH 15/1091 (1,4%). W celu uniknięcia jednego epizodu objawowej VTE należy więc stosować przedłużoną profilaktykę za pomocą LMWH u 45,3 chorych (95% CI: 25,5 – 204,5; p<0,012) [45]. Duże krwawienie wystąpiło u 1 z 862 chorych w grupie placebo (0,115%) oraz u żadnego chorego z grupy przedłużonej profilaktyki LMWH [45].
Cel pracy
Celem pracy jest ocena kosztów i efektów przedłużonej poszpitalnej profilaktyki enoksaparyną w porównaniu do profilaktyki stosowanej tylko w okresie hospitalizacji u chorych poddanych zabiegowi planowanej alloplastyki stawu biodrowego w Polsce.
Materiał i metody
Badana populacja
Badaną populację stanowią chorzy poddani planowanemu zabiegowi alloplastyki stawu biodrowego. W analizie założono, że średni wiek tych chorych wynosi około 70 lat, co zgodne jest z opinią polskich ekspertów i odpowiada charakterystyce chorych biorących udział w badaniu klinicznym wykorzystanym jako źródło danych o wynikach klinicznych porównywanych strategii [37].
Alternatywy do porównania
W badaniu porównywano dwie metody profilaktyki przeciwzakrzepowej u chorych poddanych planowej alloplastyce stawu biodrowego: enoksaparynę w dawce 40 mg 1 raz dziennie stosowaną tylko w okresie hospitalizacji (profilaktyka krótkoterminowa) oraz enoksaparynę w dawce 40 mg 1 raz dziennie stosowaną w okresie hospitalizacji i w ciągu 21 dni po wypisaniu ze szpitala (profilaktyka długoterminowa). Dawkowanie leku przyjęte w analizie było takie, jak stosowano w badaniu klinicznym stanowiącym źródło danych o skuteczności porównywanych metod profilaktyki [37] i jest ono zgodne z polskimi wytycznymi profilaktyki VTE u chorych poddanych planowemu zabiegowi alloplastyki stawu biodrowego [31,32].
Metody
W celu oszacowania kosztów i efektów przedłużonej profilaktyki enoksaparyną u chorych poddanych planowemu zabiegowi alloplastyki stawu biodrowego w Polsce skonstruowano model decyzyjny, używając DataTM 3.5 (Version 3.5.5., 1988-2000, TreeAge Software, Inc. Willimastown, Ma, USA). W modelu tym wykorzystano wyniki międzynarodowych badań klinicznych oraz dane o zużytych zasobach i kosztach jednostkowych odpowiadające praktyce klinicznej w Polsce i polskim warunkom ekonomicznym. Wykorzystanie międzynarodowych danych klinicznych było możliwe, ponieważ w przeciwieństwie do danych ekonomicznych, wyniki badań klinicznych w przypadku większości chorób nie są uważane za specyficzne dla danego kraju [38,39].
Symulując hipotetyczne badanie pragmatyczne dokonano w modelu ekstrapolacji krótkoterminowych kryteriów skuteczności (częstość występowania flebograficznie rozpoznanej DVT) do ostatecznych punktów końcowych (śmiertelność i zyskane lata życia). Zastosowanie modelu, w którym zintegrowane dane pochodzące z różnych źródeł było konieczne z powodu braku bezpośrednich polskich danych kliniczno-ekonomicznych.
Opis modelu
Schemat drzewa decyzyjnego, wykorzystanego w badaniu przedstawia rycina 1. Pierwszy węzeł drzewa decyzyjnego (węzeł decyzyjny) przedstawia wybór między stosowaniem przedłużonej profilaktyki enoksaparyną (przez 21 dni po wypisaniu chorego ze szpitala) lub jej niestosowaniem. Oba sposoby postępowania różnią się skutecznością, mierzoną ryzykiem wystąpienia DVT. Jest to kluczowa zmienna, w badaniach klinicznych mierzona za pomocą flebografii wykonywanej u wszystkich objętych badaniem pacjentów. Częstość występowania objawowej DVT w praktyce klinicznej jest o wiele mniejsza niż w badaniach klinicznych, ponieważ flebografii nie wykonuje się rutynowo u wszystkich chorych po operacji, także u tych bez objawów klinicznych. Dlatego głównym problemem przy konstruowaniu modelu profilaktyki przeciwzakrzepowej jest oszacowanie prawdopodobieństwa wystąpienia zdarzeń istotnych klinicznie na podstawie danych uzyskanych za pomocą badań przesiewowych. Wymaga to dokonania pewnych założeń, które umożliwią obliczenie, jaki odsetek zakrzepów, wykrytych za pomocą testów przesiewowych, będzie przyczyną objawowej DVT.
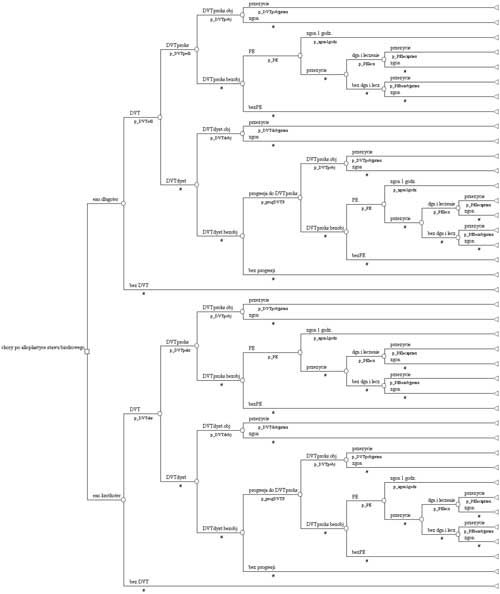
Ryc.1. Drzewo decyzyjne: profilaktyka przeciwzakrzepowa po operacji alloplastyki stawu biodrowego.
Kolejne odgałęzienia drzewa decyzyjnego przedstawiają różne potencjalne sytuacje kliniczne, będące następstwem objawowej lub bezobjawowej DVT. W modelu zawarto informacje o możliwości przemieszczenia się skrzepliny (progresja dystalnej DVT do proksymalnej, PE), rutynowym postępowaniu klinicznym w Polsce (diagnostyka i leczenie) oraz skutkach leczenia.
Postępowanie w przypadku objawowej DVT (proksymalnej lub dystalnej) polega na wykonaniu obiektywnego testu diagnostycznego i zastosowaniu leczenia przeciwzakrzepowego. W modelu założono, że wszystkie przypadki zatorowości płucnej są wynikiem nierozpoznanych i nieleczonych epizodów DVT (proksymalnej oraz dystalnej, która uległa progresji do proksymalnej). Jeśli pacjent przeżyje pierwszą godzinę i PE zostanie potwierdzony obiektywnym testem, stosuje się odpowiednie leczenie. Każde odgałęzienie drzewa decyzyjnego kończy się wynikiem ostatecznym, którym jest zgon lub przeżycie.
Prawdopodobieństwa zdarzeń
Prawdopodobieństwa zdarzeń w modelu przedstawia tabela 1. W analizie podstawowej prawdopodobieństwo stwierdzonej flebograficznie DVT w grupach z i bez profilaktyki długoterminowej (odpowiednio 0,18 vs 0,39) oraz odsetek proksymalnej DVT w porównywanych grupach (odpowiednio: 0,38 i 0,62) oszacowano na podstawie wyników badania Bergqista [37]. Wyniki dwóch pozostałych badań klinicznych, w których porównywano krótko- i długotrwałą profilaktykę enoksaparyną w populacji chorych poddanych operacji alloplastyki stawu biodrowego [40,41] wykorzystano w analizie wrażliwości w celu zbadania wpływu niższej zapadalności na DVT na wyniki analizy. Nie były one brane pod uwagę w analizie podstawowej, ponieważ w badaniu Compa i wsp. [41] dawkowanie enoksaparyny nie jest zgodne z zaleceniami polskich wytycznych profilaktyki choroby zakrzepowo-zatorowej [32,33], a w badaniu Planesa i wsp.[40] głównym kryterium kwalifikacyjnym pacjentów był potwierdzony flebograficznie brak cech zakrzepicy żył głębokich w momencie wypisu ze szpitala, co nie odpowiada rutynowej praktyce klinicznej a ponadto może być czynnikiem zakłócającym w analizie różnic pomiędzy grupą badaną i kontrolną.
Tabela 1. Prawdopodobieństwa zdarzeń w modelu.
| Parametr | Przedłużona profilaktyka | Bez przedłużonej profilaktyki | Referencje |
| DVT | 0,18 (95% CI: 0,09-0,21) | 0,39 (95% CI: 0,26-0,41) | 37 |
| DVT proksymalna | 0,38 (0,34-0,83) | 0,62 (0,5-0,64) | 37 40, 41, 45 |
| Objawowa DVT proksymalna | 0,4 | 0,4 | 46 |
| Objawowa DVT dystalna | 0,05 | 0,05 | 46 |
| Progresja bezobjawowej DVT dystalnej do DVT proksymalnej | 0,2 | 0,2 | 47. |
| PE w przypadku bezobjawowej DVT proksymalnej | 0,5 | 0,5 | 48 |
| Zgon z powodu PE w ciągu 1 godz. | 0,11 | 0,11 | 49 |
| Leczenie PE u chorych, którzy przeżyli 1 godz. | 0,29 | 0,29 | 49 |
| Zgon z powodu PE u leczonych na PE | 0,025 | 0,025 | 50 |
| Zgon z powodu PE u chorych z bezobjawowym PE | 0,3 | 0,3 | 50,51 |
| Zgon z powodu leczenia objawowej DVT | 0,0007 | 0,0007 | 52-56 |
Prawdopodobieństwo zdarzeń o znaczeniu klinicznym oszacowano na podstawie dostępnych danych literaturowych o naturalnym przebiegu VTE. W modelu przyjęto, że:
1) 40% proksymalnych DVT rozpoznaje się klinicznie [46],
2) tylko 5% dystalnych DVT przebiega z objawami klinicznymi [46],
3) 20% nierozpoznanych dystalnych zakrzepów przemieszcza się do żył proksymalnych [47].
Dane na temat prawdopodobieństwa wystąpienia PE również są ekstrapolowane z danych na temat rozpowszechnienia DVT. W publikowanych badaniach klinicznych istnieje zgodność co do tego, że tylko proksymalna DVT może rozwinąć się do PE. Szacuje się, że 50% proksymalnych DVT kończy się PE [48], a 11% chorych umiera w ciągu pierwszej godziny po wystąpienia PE [49]. U około 29% chorych, którzy przeżyją, rozpoznanie potwierdzone zostaje obiektywnym testem i wdrożone jest leczenie [49]. Około 2,5% tych chorych umiera [50]. Śmiertelność wśród pacjentów z bezobjawowym PE wynosi 30% [50,51]. Ryzyko zgonu z powodu powikłań krwotocznych leczenia przeciwzakrzepowego u chorych z DVT wynosi 0,0007 [52-56].
Oczekiwane przeżycie
Liczbę zyskanych lat życia w wyniku zastosowania przedłużonej profilaktyki enoksaparyną obliczono, mnożąc liczbę unikniętych zgonów (różnica prawdopodobieństwa przeżycia w porównywanych grupach) przez oczekiwane przeżycie. Ponieważ wiek badanej populacji wynosił średnio 70 lat, a udział mężczyzn i kobiet wynosił odpowiednio 42% i 58% [37], na podstawie polskich danych statystycznych przyjęto, że oczekiwane przeżycie wynosi 12,8 lat [57].
Koszty
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. National Institutes of Health Consensus Conference. Prevention of venous thrombosis and pulmonary embolism. JAMA, 1986, 256, 744-9.
2. Hull, RD, Pineo, GF. Clinical features of deep venous thrombosis. W: Hull, RD Raskob, GE Pineo, GF eds. VTE: an evidence-based atlas,87-91 Futura Publishing Armonk, NY. 1996.
3. Stein, PD. The clinical diagnosis of acute pulmonary embolism. Hull, RD Raskob, GE Pineo, GF eds. VTE: an evidence-based atlas,161-167 Futura Publishing Armonk, NY. 1996.
4. Franzeck, UK, Schalch, I, Jager, KA, et al. Prospective 12-year follow-up study of clinical and hemodynamic sequelae after deep vein thrombosis in low-risk patients (Zurich study). Circulation 1996; 93:74-79.
5. Prandoni, P, Lensing, AWA, Cogo, A, et al. The long-term clinical course of acute deep venous thrombosis. Ann Intern Med 1996; 125:1-7.
6. Seagroatt V, Tan ST, Goldacre M, et al. Elective total hip replacement: incidence, emergency readmission, and postoperative mortality. BMJ 1991; 303: 1431-5.
7. Flordal, PA, Bergqvist, D, Burmark, U-S, et al. Risk factors for major thromboembolism and bleeding tendency after elective general surgical operations. Eur J Surg 1996; 162:783-789.
8. Brandjes, DPM, ten Cate, JW, Buller, HR. Pre-surgical identification of the patient at risk for developing VTE post-operatively. Acta Chir Scand 1990; 556(suppl):18-21.
9. Caprini, JA, Arcelus, JI, Hasty, JH, et al. Clinical assessment of thromboembolic risk in surgical patients. Semin Thromb Hemost 1991; 17(suppl 3):304-312.
10. Thromboembolic Risk Factors (THRIFT) Consensus Group. Risk of and prophylaxis for VTE in hospital patients. BMJ 1992; 305:567-574.
11. Nicolaides, AN, Bergqvist, D, Hull, R, et al. Prevention of VTE: international consensus statement (guidelines according to scientific evidence). Int Angiol 1997;16: 3-38
12. Clagett, GP, Anderson, FA, Geerts, W, et al. Prevention of VTE. Chest 1998; 114(suppl):531S-560S.
13. Thromboembolic Risk Factors (THRiFT II) Consensus Group. Risk of and prophylaxis for VTE in hospital patients. Phlebology 1998; 13:87-97.
14. Gallus, A, Raman, K, Darby, T. Venous thrombosis after elective hip replacement - the influence of preventive intermittent calf compression and of surgical technique. Br J Surg 1983; 70:17-19.
15. Turpie, AGG, Levine, MN, Hirsh, J, et al. A randomized controlled trial of a low-molecular-weight heparin (enoxaparin) to prevent deep-vein thrombosis in patients undergoing elective hip surgery. N Engl J Med 1989; 315:925-929.
16. Hull, RD, Raskob, GE, Gent, M, et al. Effectiveness of intermittent pneumatic leg compression for preventing deep vein thrombosis after total hip replacement. JAMA 1990; 263:2313-2317.
17. Hoek, JA, Nurmohamed, MT, Hamelynck, KJ, et al. Prevention of deep vein thrombosis following total hip replacement by low molecular weight heparinoid. Thromb Haemost 1992; 67:28-32.
18. Moskovitz, PA, Ellenberg, SS, Feffer, HL, et al. Low-dose heparin for prevention of VTE in total hip arthroplasty and surgical repair of hip fractures. J Bone Joint Surg Am 1978; 60:1065-1070.
19. Evarts, CM, Feil, EJ. Prevention of thromboembolic disease after elective surgery of the hip. J Bone Joint Surg Am 1971; 53:1271-1280.
20. Cooke, ED, Dawson, MHO, Ibbotson, RM, et al. Failure of orally administered hydroxychloroquine sulphate to prevent VTE following elective hip operations. J Bone Joint Surg 1977; 59: 496-500.
21. Harris, WH, Salzman, EW, Athanasoulis, CA, et al. Aspirin prophylaxis of VTE after total hip replacement. N Engl J Med 1977; 297:1246-1249.
22. Rogers, PH, Walsh, PN, Marder, VJ, et al. Controlled trial of low-dose heparin and sulfinpyrazone to prevent VTE after operation of the hip. J Bone Joint Surg 1978; 60-A:758-762.
23. Belch, JJF, Meek, DR, Lowe, GDO, et al. Subcutaneous ancrod in prevention of deep vein thrombosis after hip replacement surgery. Thromb Res 1982; 25:23-31.
24. Beisaw, NE, Comerota, AJ, Groth, HE, et al. Dihydroergotamine/heparin in the prevention of deep-vein thrombosis after total hip replacement: a controlled, prospective, randomized multicenter trial. J Bone Joint Surg 1988; 70-A:2-10.
25. Kalodiki, EP, Hoppensteadt, DA, Nicholaides, AN, et al. Deep venous thrombosis prophylaxis with low molecular weight heparin and elastic compression in patients having total hip replacement: a randomised controlled trial. Int Angiology 1996; 15:162-168.
26. Eriksson, BI, Kälebo, P, Anthmyr, BA, et al. Prevention of deep-vein thrombosis and pulmonary embolism after total hip replacement: comparison of low-molecular-weight heparin and unfractionated heparin. J Bone Joint Surg Am 1991; 73:484-493.
27. Dahl, OE, Andreassen, G, Aspelin, T, et al. Prolonged thromboprophylaxis following hip replacement surgery - results of a double-blind, prospective, randomised, placebo-controlled study with dalteparin (Fragmin). Thromb Haemost 1997; 77:26-31.
28. Planes, A, Vochelle, N, Darmon, J-Y, et al. Risk of deep-venous thrombosis after hospital discharge in patients having undergone total hip replacement: double-blind randomised comparison of enoxaparin versus placebo. Lancet 1996; 348:224-228.
29. Hull, RD, Pineo, GF, Francis, CW, et al. Low-molecular-weight heparin prophylaxis using dalteparin extended out- of- hospital warfarin versus out-of-hospital placebo in hip arthroplasty patients. A double-blind, randomized comparison. Arch Intern Med 2000; 160:2208-2215.
30. Warwick, D, Williams, MH, Bannister, GC. Death and thromboembolic disease after total hip replacement: a series of 1162 cases with no routine chemical prophylaxis. J Bone Joint Surg Br 1995; 77:6-10.
31. Geerst WH, Heit JA, Clagett GP, Pineo GF, et al. Prevention of venous thromboembolism. Sixth ACCP Consensus Conference on Antithrombotic Therapy. http://www.chestnet.org/guidelines/antithrombotic/p8.php. available: 1.05.2003.
32. Wytyczne profilaktyki i leczenia żylnej choroby zakrzepowo-zatorowej. Medycyna praktyczna 2002 suplement 5(135): 3-26.
33. Polska Grupa Robocza d/s Profilaktyki Przeciwzakrzepowej w Ortopedii. Zasady profilaktyki żylnej choroby zakrzepowo-zatorowej w ortopedii i traumatologii narządu ruchu. "Ortopedia, Traumatologia, Rehabilitacja" Vol 5 Nr 1, 2003, 123-126.
34. Berqvist D, Joensson B. Cost-effectiveness of prolonged administration of a low molecular weight heparin for the prevention of deep venous thrombosis following total hip replacement. Value in Health 1999; 4(2): 288-294.
35. Detournay B, Planes A, Vochelle N, et al. Cost-effectiveness of a low molecular weight heparin in prophylaxis against deep venous thrombosis following total hip replacement. Pharmacoeconomics 1998; 13(1):81-9.
36. Davies LM, Richardson GA, et al. Economic evaluation of enoxaparin as postdischarge prophylaxis for deep venous thrombosis (DVT) in elective hip surgery. Value in Health 2000; 6(3): 397-406.
37. Bergqvist D, Benoni G, Bjorgell O, et al. Low molecular weight heparin (enoxaparin) as prophylaxis against deep vein thrombosis after total hip replacement. N Engl J Med 1996; 335: 697-700.
38. Nuijten MJC. Data management in modeling studies: the selection of data sources. Pharmacoeconomics 1998; 3: 305-16.
39. Orlewska E., Mierzejewski P. Polskie wytyczne przeprowadzania badań farmakoekonomicznych (projekt). Farmakoeonomika 2000; Suplement 1:3-11.
40. Planes A, Vochelle N, Darmon JY, et al. Risk of deep venous thrombosis after hospital discharge in patients having undergone total hip replacement: double blind randomized comparison of enoxaparin versus placebo. Lancet 1996; 348(9022): 224-8.
41. Comp PC, Spiro TE, et al. Prolonged enoxaparin therapy to prevent venous thromboembolism after primary hip or knee replacement. Enoxaparin Clinical Trial Group. J Bone Joint Surg Am 2001 Mar;83-A(3):336-45
42. Dahl OE, AndreasseG, et al. Prolonged thromboporphylaxis following total hip replacement surgery - results of a double-blind, prospective, randomized, placebo controlled study with dalteparin (Fragmin). Thromb Haemostat 1997; 77: 26-31.
43. Lassen MR, Borris LC, et al. Efficacy and safety of prolonged thromboprophylaxis with a low molecular weight heparin (dalteparin) after total hip arthroplasty - the Danish Prolonged prophylaxis (DaPP) Study. Thromb Res 1998; 89: 281-87.
44. Hull RD, Pineo GF, Francis C, et al. Low-molecular-weight heparin prophylaxis using dalteparin extended out-of-hospital vs in-hospital warfarin/out-of-hospital placebo in hip arthroplasty patients: a double-blind, randomized comparison. North American Fragmin Trial Investigatots. Arch Intern Med 2000; 160: 2208-15.
45. Hull RD, Pineo GF, et al. Extended out-of-hospital low-molecular-weight heparin prophylaxis against deep venous thrombosis in patients after elective hip atrhroplasty: a systematic review. Ann Intern Med 2001; 135: 858-69.
46. Gallus AS. Venous thromboembolism: incident and clinical risk factors. In Madden JL, Hume M (eds): Venous thromboembolism: Prevention and treatment, Appleton-Century-Crofts, East Norwalk, Conn, 1976: 1-32.
47. Oster G, Tudden RL, Colditz GA. A cost-effectiveness analysis of prophylaxis against deep-vein thrombosis in major orthopedic surgery. JAMA 1987; 257: 203-208.
48. Kakkar VV, Flanc C, Howe CT, et al. Natural history of postoperative deep vein thrombosis. Lancet 1969; 2: 230-233.
49. Dalen JE, Alpert JS. Natural history of pulmonary embolism. Prog Cardiovasc Dis 1975; 17: 259-270.
50. Carson JL, Kelley MA, et al. The clinical course of pulmonary embolism. N Engl J Med 1992; 17: 1240-1245
51. Egermayer P. Value of anticoagulants in the treatment of pulmonary embolism. J R Soc Med 1981; 74:675-681
52. Levine MN, Hirsch J, et al. Hemorrhagic complications of anticoagulant treatment.Chest 1992; 102:352-263
53. Hull RD, Raskob GE, et al. Subcutaneous low-molecular weight heparin compared with intravenous heparin in the treatment of proximal vein thrombosis. N Engl J Med 1992; 326: 975-982.
54. Gallus A, Jackaman J, et al. Safety and efficacy of warfarin started early after submassive venous thrombosis or pulmonary embolism. Lancet 1986; 2:1293-1300.
55. Prandoni P, Lensing AWA, et al. Comparison of subcutaneous low-molecular-weight heparin with intravenous standard heparin in proximal deep-vein thrombosis. Lancet 1992; 339:441-445.
56. Hull RD, Raskob G, et al. Heparin for 5 days compared with 10 days in the initial treatment of proximal venous thrombosis. N Engl J Med 1990; 322: 1260-1264.
57. Główny Urząd Statystyczny. Tabele przeżycia 2001. www.stat.gov.pl/serwis/nieregularne/trwanie_tabl.xls.
58. Taryfikator usług medycznych 2002. www.kasa_chorych,lodx.pl/Konkurs2002/cennik.html
59. Standardowe koszty świadczeń medycznych. Farmakoekonomika 2003 1(6):
60. Standarodwe koszty świadczeń medycznych. Farmakoekonomika 2003 Suplement 1: 1-24.
61. Cennik leków hurtowni CEFARM 2002.
62. Orlewska E. Analiza koszty-efektywność stosowania preparatu Arthrotec 75 vs diklofenak SR 75 u chorych z reumatoidalnym zapaleniem stawów w Polsce. Farmakoekonomika 2000; 1: 2-19.

