*Łukasz Słowik1, Aleksy Nowak1, Maciej Okła1, Zuzanna Ślebioda2, Krzysztof Osmola1, Ewa Totoń3
Opieka stomatologiczna nad pacjentem z grupy ryzyka martwicy kości szczęk w gabinecie stomatologicznym
Dental care for a patient at risk of osteonecrosis of the jaws in a dental practice
1Katedra i Klinika Chirurgii Szczękowo-Twarzowej, Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu
Kierownik Kliniki: dr hab. Krzysztof Osmola
2Katedra i Klinika Chirurgii Stomatologicznej i Periodontologii, Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu
Kierownik Kliniki: prof. dr hab. Marzena Wyganowska-Świątkowska
3Katedra i Zakład Chemii Klinicznej i Diagnostyki Molekularnej, Uniwersytet Medyczny im. K. Marcinkowskiego w Poznaniu
Kierownik Katedry: prof. dr hab. Błażej Rubiś
Streszczenie
U pacjentów stomatologicznych zapaleniem kości nazywamy niejednorodną grupę chorób, których skutkiem jest postępujące niszczenie struktury kostnej szczęki i żuchwy w wyniku toczącego się procesu zapalnego. W efekcie nieleczonego procesu zapalnego dochodzi do martwicy tkanki kostnej. Wśród zmian zapalnych kości szczękowych największą grupę stanowią poradiacyjne zapalenia i zmiany polekowe w wyniku długotrwałego leczenia onkologicznego. Zapalenia kości poradiacyjne w populacji dzieci i młodzieży dotyczą głównie kości długich. Wśród młodszych pacjentów przyjmujących leki antyresorpcyjne nie opisano przypadków martwicy kości.
Utrwalona wiedza obejmująca znajomość czynników zwiększających ryzyko zapalenia kości obszaru szczękowego oraz prawidłowo prowadzona przez lekarzy stomatologów profilaktyka przyczyniają się do eliminowania tego trudnego w leczeniu powikłania. Celem niniejszej pracy jest przedstawienie charakterystyki schorzenia, jego etiologii, czynników ryzyka i schematu postępowania okołozabiegowego według wytycznych Grupy Roboczej Polskiego Towarzystwa Stomatologicznego oraz Narodowego Programu Ochrony Antybiotyków.
Summary
In dental patients, osteomyelitis is a heterogeneous group of diseases that result in non-healing, progressive destruction of the jaw and mandible as a result of the ongoing inflammatory process. As a result of the untreated inflammatory process, bone tissue necrosis occurs. Among the inflammatory lesions of the jaws, the largest group are radiation- and drug-induced lesions as a result of long-term oncological treatment. In the pediatric population, osteitis after radiotherapy mainly affects long bones. There have been no reports of drug induced osteonecrosis in younger patients.
Knowledge, including the factors increasing the risk of osteomyelitis in the maxillary area and prophylaxis, carried out correctly by dentists, contribute to the elimination of this difficult-to-treat complication. This study aims to present the characteristics of the disease, its etiology, and risk factors. This study shows the perioperative procedure according to the guidelines of the Working Group of the Polish Dental Society and the National Program for the Protection of Antibiotics.

Wstęp
Kość jest aktywną metabolicznie tkanką charakteryzującą się ciągłą przebudową, opartą na dwóch przeciwstawnych procesach: resorpcji i tworzeniu. Obrót kostny zapewnia zachowanie integralnej struktury kości, wymianę jej składników z płynami ustrojowymi oraz naprawę mikrouszkodzeń (1). Dzięki temu tkanka kostna cechuje się znacznym potencjałem gojenia. Każda ekstrakcja zęba, przeprowadzona nawet atraumatycznie, uruchamia procesy gojenia kości. Gojenie wyrostka zębodołowego w odróżnieniu od gojenia kości długich następuje z pominięciem gojenia śródchrzęstnego i zachodzi w środowisku obfitym w mikroorganizmy (2). Procesy infekcyjne występujące po ekstrakcji zębów są jedną z przyczyn zaburzeń gojenia mogących skutkować zapaleniem kości obszaru szczękowego.
Zapalenie kości (osteomyelitis) w obrębie jamy ustnej jest procesem chorobowym dotyczącym wszystkich części składowych kości. Objawami przewlekłego zapalenia kości szczękowych są: dotkliwy ból kostny, obrzęk tkanek miękkich, osłabienie i łagodna gorączka (3). Konsekwencją nieleczonego procesu zapalnego jest martwica tkanki kostnej (osteonecrosis) oraz wytworzenie wysięku ropnego, który rozprzestrzeniając się naczyniami, prowadzi do poważnych zaburzeń i deformacji w obrębie kości. Wśród najczęstszych przyczyn zapalenia kości szczęki i żuchwy wymienia się: infekcje zębopochodne, poradiacyjne zapalenia oraz zmiany polekowe w terapii leczenia onkologicznego (4). Zapalenia kości bez uchwytnej przyczyny opisywane są rzadko.
Radio- i chemioterapia wywierają ogromny, ujemny wpływ na procesy gojenia kości. Radioterapia zmniejsza liczbę komórek osteogennych, zmienia aktywność cytokin, opóźnia i upośledza przebudowę kości (5). Z kolei niektóre leki stosowane w chemioterapii modelują metabolizm układu kostnego, uniemożliwiając proces resorpcji kości, który jest niezbędnym elementem jej gojenia i przebudowy. Próby poznania mechanizmu prowadzącego do zapalenia kości szczękowych skutkowały powstawaniem teorii tłumaczących zaburzenia gojenia. Teoria niedokrwienno-infekcyjna Marxa, historycznie pierwsza, powstanie choroby przypisywała zmniejszeniu ukrwienia, obniżeniu penetracji komórkowej i ograniczeniu proliferacji naczyniowej (6). Nowsza, przedstawiona w 2004 roku, teoria poradiacyjna włókniejąco-zanikowa Delaniana i Lefaix przypisuje powstanie martwicy żuchwy (ang. ostenecrosis of the jaw – ONJ) procesowi zapalnemu, wolnym rodnikom, dysfunkcji śródbłonka, zakrzepicy mikronaczyniowej i zwłóknieniu tkanek (7). Do polekowych teorii uzasadniających zaburzenia gojenia kości szczękowych należy zaliczyć teorię zewnątrz-wewnętrzną i wewnątrz-zewnętrzną (8). Obie opierają się na utracie homeostazy w obrębie tkanki kostnej wywołanej długim stosowaniem leków w terapii onkologicznej.
Martwica kości w układzie stomatognatycznym
Martwica kości szczęki i żuchwy, zwana również osteonekrozą szczęki i żuchwy, jest schorzeniem bardzo rzadkim, ale związanym z licznymi dolegliwościami podmiotowymi i przedmiotowymi. Do objawów prodromalnych należą nieznacznie nasilony ból i obrzęk. Wraz z rozwojem choroby dochodzi do pogłębienia objawów bólowych, zaburzeniu ulega gojenie zębodołów po ekstrakcji zębów. Nasileniu ulega stan zapalny okolicznych tkanek, czemu towarzyszy uczucie pieczenia lub mrowienia. W konsekwencji dochodzi do odsłonięcia kości i powstawania przetok skórnych i dziąsłowych. W stanach zaawansowanych może dojść do rozchwiania zębów oraz patologicznych złamań kości. Często w badaniu radiologicznym widoczne są martwiaki, natomiast w badaniu mikrobiologicznym stwierdzamy najczęściej obecność bakterii, m.in.: Staphylococcus epidermidis, Morganella morganii, Prevotella intermedia i Escherichia coli (9). Patologiczne zmiany tego typu mają często przewlekły charakter, co powoduje, że schorzenie to jest wysoce nieestetyczne, uciążliwe i znacząco negatywnie wpływa na komfort życia psychicznego pacjenta.
Do najczęstszych czynników predysponujących do powstania zmian zapalnych w obrębie jamy ustnej prowadzących do osteonekrozy kości szczęki i żuchwy zalicza się zabiegi na wyrostku zębodołowym, zakażenia bakteryjne, naświetlania okolicy głowy i szyi w terapii przeciwnowotworowej oraz powikłania terapii antyresorpcyjnej i antyangiogennej w leczeniu onkologicznym (10) (ryc. 1).
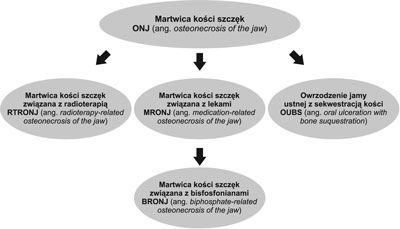
Ryc. 1. Klasyfikacja martwicy kości szczęk w oparciu o powikłania terapii onkologicznej (rycina własna wykonana na podstawie dostępnego piśmiennictwa)
Martwica kości szczęk związana z radioterapią
Popromieniozależna martwica kości szczęk (RTRONJ) występuje u około 9% pacjentów poddanych radioterapii w zakresie głowy i szyi (11). Czynniki ryzyka martwicy popromiennej mają charakter ogólnoustrojowy i miejscowy. Do głównych czynników ogólnoustrojowych zaliczamy: niedożywienie, niedobory odporności i zażywane używki (alkohol, palenie tytoniu). Wśród czynników miejscowych nadrzędną rolę odgrywa wielkość i umiejscowienie guza nowotworowego poddanego radioterapii. Dowiedziono, że wystąpienie promieniozależnej martwicy kości szczęk bezpośrednio koreluje z zastosowaną dawką promieniowania (powyżej 7000 cGy) oraz wiekiem chorego (powyżej 55. roku życia) (11).
Ponadto do istotnych czynników ryzyka martwicy popromiennej, z punktu widzenia stomatologa praktyka, należą również zabiegi z dziedziny chirurgii zębowo-wyrostkowej stosowane w trakcie radioterapii. W zagranicznych publikacjach istnieje rozbieżność odnośnie do czasu wykonywania ekstrakcji po radioterapii. Część autorów zaleca, aby w trakcie radioterapii, jak również do 12 miesięcy po jej zakończeniu, nie przeprowadzać ekstrakcji zębów ze względu na to, że zębodół po usunięciu zęba może stanowić wrota infekcji, która następnie przeniesie się na kość (12). W przeglądzie systematycznym dokonanym przez Beaumont i wsp. nie zauważono statystycznej różnicy ryzyka RTRONJ między grupą pacjentów, u których wykonano ekstrakcję przed radioterapią i po niej (13). Część autorów zwraca uwagę na bimodalny wzorzec zagrożenia martwicy kości i wskazuje dwa szczyty ryzyka – do 12 miesięcy po RT i 24-60 miesięcy od RT (14). Publikacje zagraniczne wskazują na zwiększone ryzyko martwicy kości na tle poekstrakcyjnym po 2 latach od radioterapii w porównaniu z interwencją chirurgiczną do roku po niej (15). Przedstawione przypisy ukazują brak jednoznacznych wytycznych odnośnie do bezpiecznego czasu ekstrakcji zębów. Zagraniczni autorzy wskazują, że czynnikiem, na który ma wpływ lekarz dentysta, jest przeprowadzenie zabiegu atraumatycznie celem eliminacji ogniska zapalnego (16). Ostre zębopochodne stany zapalne w postaci ropni okołoszczękowych mogą skutkować pogorszeniem ogólnego stanu chorego i wymagać leczenia szpitalnego.
Równie ważnym, a często bagatelizowanym, czynnikiem ryzyka wystąpienia martwicy kości szczęk u pacjentów poddawanych radioterapii są źle dopasowane protezy. Stomatolog prowadzący pacjenta powinien zadbać o ich odpowiednią adaptację przed rozpoczęciem naświetlań. W przypadku konieczności wykonania nowych protez zaleca się ową czynność przeprowadzić dopiero po upływie przynajmniej 6 miesięcy od zakończenia radioterapii (17).
Martwica kości szczęk związana z lekami
Powyżej zamieściliśmy fragment artykułu, do którego możesz uzyskać pełny dostęp.
Mam kod dostępu
- Aby uzyskać płatny dostęp do pełnej treści powyższego artykułu albo wszystkich artykułów (w zależności od wybranej opcji), należy wprowadzić kod.
- Wprowadzając kod, akceptują Państwo treść Regulaminu oraz potwierdzają zapoznanie się z nim.
- Aby kupić kod proszę skorzystać z jednej z poniższych opcji.
Opcja #1
29 zł
Wybieram
- dostęp do tego artykułu
- dostęp na 7 dni
uzyskany kod musi być wprowadzony na stronie artykułu, do którego został wykupiony
Opcja #2
69 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 30 dni
- najpopularniejsza opcja
Opcja #3
129 zł
Wybieram
- dostęp do tego i pozostałych ponad 7000 artykułów
- dostęp na 90 dni
- oszczędzasz 78 zł
Piśmiennictwo
1. Hadjidakis DJ, Androulakis II: Bone remodeling. Ann N Y Acad Sci 2006; 1092: 385-396.
2. Vieira AE, Repeke CE, Ferreira Junior Sde B et al.: Intramembranous bone healing process subsequent to tooth extraction in mice: micro-computed tomography, histomorphometric and molecular characterization. PLoS One 2015; 10(5): e0128021.
3. Mark AM: What Is MRONJ? For the Patient 2021; 1552(8): 710.
4. Wan JT, Sheeley DM, Somerman MJ et al.: Mitigating osteonecrosis of the jaw (ONJ) through preventive dental care and understanding of risk factors. Bone Resarch 2020; 14(8).
5. Jegoux F, Malard O, Goyenvalle E et al.: Radiation effects on bone healing and reconstruction: interpretation of the literature. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2010; 109(2): 173-184.
6. Marx RE: Osteoradionecrosis: a new concept of its pathophysiology. J Oral Maxillofac Surg 1983; 41(5): 283-288.
7. Delanian S, Lefaix JL: The radiation-induced fibroatrophic process: therapeutic perspective via the antioxidant pathway. Radiother Oncol 2004; 73(2): 119-131.
8. Lombard T, Neirinckx V, Rogister B et al.: Medication-Related Osteonecrosis of the Jaw: New Insights into Molecular Mechanisms and Cellular Therapeutic Approaches. Stem Cells Int 2016; 2016: 8768162.
9. Mariotti A: Bisphosphonates and osteonecrosis of the jaws. J Dent Educ 2008; 72(8): 919-929.
10. Mallya SM, Tetradis S: Imaging of Radiation- and Medication-Related Osteonecrosis. Radiol Clin North Am 2018; 56(1): 77-89.
11. Davis DD, Hanley ME, Cooper JS: Osteoradionecrosis. 2022, StatPearls Publishing LLC.
12. Chrcanovic BR, Reher P, Sousa, AA et al.: Osteoradionecrosis of the jaws – a current overview. Part 2: dental management and therapeutic options for treatment. Oral and Maxillofacial Surgery 2010; 14: 81-95.
13. Beaumont S, Bhatia N, McDowell L et al.: Timing of dental extractions in patients undergoing radiotherapy and the incidence of osteoradionecrosis: a systematic review and meta-analysis. Br J Oral Maxillofac Surg 2021; 59(5): 511-523.
14. Marx R, Johnson R: Studies in the radiobiology of osteoradionecrosis and their clinical significance. Oral Surg Oral Med Oral Pathol 1987; 64: 379-390.
15. Nabil S, Samman N: Incidence and prevention of osteoradionecrosis after dental extraction in irradiated patients: a systematic review. Int J Oral Maxillofac Surg 2011; 40(3): 229-243.
16. Murdoch-Kinch CA, Zwetchkenbaum S: Dental management of the head and neck cancer patient treated with radiation therapy. Mich J Dent Assoc 2011; 93(7): 28-37.
17. Rahman RA, Ngeow WC, Chai WL et al.: Managing complications of radiation therapy in head and neck cancer patients: Part III. Provision of dentures. Singapore Dental Journal 2007; 28(1): 7-10.
18. Fehm T, Beck V, Banys M et al.: Bisphosphonate-induced osteonecrosis of the jaw (ONJ): Incidence and risk factors in patients with breast cancer and gynecological malignancies. Gynecol Oncol 2009; 112(3): 605-609.
19. Singar S, Parihar AP, Reddy P et al.: Medication-related osteonecrosis of the jaw: A review about etiology, risk factors, pathophysiology, and treatment. J Indian Acad Oral Med Radiol 2020; 32: 50-54.
20. Hoff AO, Toth BB, Altundag K et al.: Frequency and risk factors associated with osteonecrosis of the jaw in cancer patients treated with intravenous bisphosphonates. J Bone Miner Res 2008; 23(6): 826-836.
21. Reich W, Bilkenroth U, Schubert J et al.: Surgical treatment of bisphosphonate-associated osteonecrosis: Prognostic score and long-term results. J Craniomaxillofac Surg 2015; 43(9): 1809-1822.
22. Grisar K, Schol M, Schoenaers J et al.: Osteoradionecrosis and medication-related osteonecrosis of the jaw: similarities and differences. Int J Oral Maxillofac Surg 2016; 45(12): 1592-1599.
23. Khan AA, Morrison A, Hanley DA et al.: International Task Force on Osteonecrosis of the Jaw. Diagnosis and management of osteonecrosis of the jaw: a systematic review and international consensus. J Bone Miner Res 2015; 30(1): 3-23.
24. Lidhar T, Ethunandan A, Ethunandan M: Spontaneous oral ulceration with bone sequestration: its relevance in current clinical practice. Br J Oral Maxillofac Surg 2020; 58(9): e75-e79.
25. Di Fede O, Panzarella V, Mauceri R et al.: The Dental Management of Patients at Risk of Medication-Related Osteonecrosis of the Jaw: New Paradigm of Primary Prevention. Biomed Res Int 2018; 2018: 2684924.
26. Palla B, Burian E, Klecker JR et al.: Systematic review of oral ulceration with bone sequestration. J Craniomaxillofac Surg 2016; 44(3): 257-264.
27. Rekomendacje Grupy Roboczej Polskiego Towarzystwa Stomatologicznego i Narodowego Programu Ochrony Antybiotyków w zakresie stosowania antybiotyków w stomatologii; http://antybiotyki.edu.pl/wp-content/uploads/2019/01/stomatologia-zalecenia-25_01-net.pdf.
28. Bermúdez-Bejarano EB, Serrera-Figallo MA, Gutièrrez-Corrales A et al.: Prophylaxis and antibiotic therapy in management protocols of patients treated with oral and intravenous bisphosphonates. J Clin Exp Dent 2017; 9(1): e141-e149.
29. Shrestha A, Martin C, Burton M et al.: Quality of life versus length of life considerations in cancer patients: A systematic literature review. Psychooncology 2019; 28(7): 1367-1380.
30. Reuther T, Schuster T, Mende U et al.: Osteoradionecrosis of the jaws as a side effect of radiotherapy of head and neck tumour patients – a report of a thirty year retrospective review. Int J Oral Maxillofac Surg 2003; 32(3): 289-295.
31. Sennhenn-Kirchner S, Freund F, Grundmann S et al.: Dental therapy before and after radiotherapy – an evaluation on patients with head and neck malignancies. Clin Oral Investig 2009; 13(2): 157-164.


